acquaRIeuno | Caridine, piante, muschi e fai da te
- Home
- I miei acquari
- Fai da te
-
Caridine
- Anatomia
- Alimentazione
- Dimorfismo sessuale e riproduzione
- Il caridinaio e i parametri ideali
- L'ambientamento delle caridine e gli accessori
- La classificazione e la selezione - DAVIDI...
- La classificazione e la selezione - LOGEMANNI
- La classificazione e la selezione - MARIAE
- La classificazione e la selezione - TAIWAN BEE
- Piante e Muschi
- CHIMICA
- ABOUT
Tossicita' e letalita' dell'ammoniaca
Partiamo da una premessa importante:
l’azoto ammoniacale e nitroso risulta tossico non solo per gli animali in acquario ma anche per gli stessi batteri nitrificanti. Anche in letteratura scientifica risulta che l’attività nitrificante dei batteri è estremamente bassa in presenza di elevate quantità di ioni ammonio e nitrito (Bower e Turner, 1983; Yang et al., 1995; Sakairi et al., 1996).
La tossicità dell’ammoniaca indissociata per i batteri del genere Nitrosomonas risulta compresa tra 10-150 ppm, mentre per i Nitrobacter è più sensibile, 0,1 ppm. L’azoto nitroso risulta tossico a 1 ppm (Saroglia, 2001).
Comunemente, fra i principianti, si parla di ammoniaca senza fare alcuna distinzione fra ammoniaca (NH3) e ione ammonio (NH4), probabilmente perché si fa riferimento ai test commerciali.
I comuni test per acquario non riescono a misurare entrambe le forme dell’ammoniaca, in modo distinto, ma misurano il valore totale delle due, quindi l’ammoniaca totale (NH3 + NH4 ovvero TAN – Total Ammonia Nitrogeno).
Entrambe le forme sono dannose, ma l’ammoniaca NH3 è quella più pericolosa per i nostri animali.
Esiste una correlazione molto stretta tra PH, temperatura e ammoniaca.
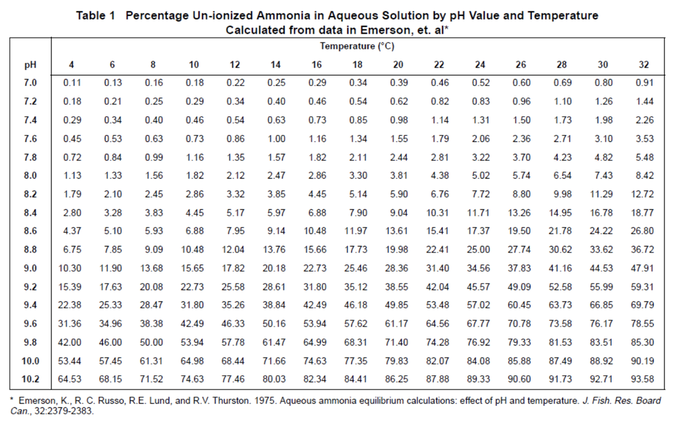
La percentuale di ammoniaca (NH3) presente in vasca aumenta con PH alcalino (uguale o superiore a 7) e la stessa cosa accade con l’aumentare della temperatura.
Attenzione però, la correlazione è molto più forte con il PH piuttosto che con la temperatura. L’aumento della temperatura, infatti, comporta un minimo aumento di concentrazione di ammoniaca rispetto all’aumento causato da un PH più alcalino.
Un aumento di un'unità di PH aumenterà la concentrazione di NH3 di circa 10 volte!
La tabella di seguito chiarisce questa correlazione.
l’azoto ammoniacale e nitroso risulta tossico non solo per gli animali in acquario ma anche per gli stessi batteri nitrificanti. Anche in letteratura scientifica risulta che l’attività nitrificante dei batteri è estremamente bassa in presenza di elevate quantità di ioni ammonio e nitrito (Bower e Turner, 1983; Yang et al., 1995; Sakairi et al., 1996).
La tossicità dell’ammoniaca indissociata per i batteri del genere Nitrosomonas risulta compresa tra 10-150 ppm, mentre per i Nitrobacter è più sensibile, 0,1 ppm. L’azoto nitroso risulta tossico a 1 ppm (Saroglia, 2001).
Comunemente, fra i principianti, si parla di ammoniaca senza fare alcuna distinzione fra ammoniaca (NH3) e ione ammonio (NH4), probabilmente perché si fa riferimento ai test commerciali.
I comuni test per acquario non riescono a misurare entrambe le forme dell’ammoniaca, in modo distinto, ma misurano il valore totale delle due, quindi l’ammoniaca totale (NH3 + NH4 ovvero TAN – Total Ammonia Nitrogeno).
Entrambe le forme sono dannose, ma l’ammoniaca NH3 è quella più pericolosa per i nostri animali.
Esiste una correlazione molto stretta tra PH, temperatura e ammoniaca.
La percentuale di ammoniaca (NH3) presente in vasca aumenta con PH alcalino (uguale o superiore a 7) e la stessa cosa accade con l’aumentare della temperatura.
Attenzione però, la correlazione è molto più forte con il PH piuttosto che con la temperatura. L’aumento della temperatura, infatti, comporta un minimo aumento di concentrazione di ammoniaca rispetto all’aumento causato da un PH più alcalino.
Un aumento di un'unità di PH aumenterà la concentrazione di NH3 di circa 10 volte!
La tabella di seguito chiarisce questa correlazione.
In base alla tabella che vi ho appena mostrato possiamo tranquillamente affermare che avremo più ammoniaca a PH elevato. Quindi verrebbe da pensare che dovremmo preoccuparci di monitorare la concentrazione di ammoniaca qualora avessimo una vasca con un PH e una temperatura molto alti (pensate a chi ha allestito un biotopo del Lago Tanganica).
Vi sono degli studi, però, che dimostrano come a PH acido sia necessario meno NH3 per produrre i suoi effetti tossici!
Questo vuol dire che dobbiamo monitorare anche e soprattutto le vasche con PH acidi (5,5-6,5) e temperature medie (18-23°C); vasche come quelle delle nostre caridine.
Nell’allevamento dei gamberi, per molte specie, è necessario dotarsi di un fondo allofano. La capacità tampone del fondo ci permetterà di avere un KH a 0, max 1 e il PH di solito si attesta su valori abbastanza bassi, quindi su valori di acidità, tra 5,5 e 6,5.
Si tratta di fattori molto importanti e che influiscono in modo determinante nella gestione.
Mantenere il PH e il KH bassi può essere però pericoloso e bisogna quindi adottare comportamenti idonei a evitare incidenti di percorso. Una semplice procedura come un repentino cambio con acqua a PH leggermente più elevato può provocare una conversione immediata dell'ammonio (NH4) in ammoniaca mortale (NH3) con risultati disastrosi.
Di seguito una tabella che riporta i risultati di uno studio su una specie di salmone piuttosto delicato e sensibile (EPA, 1985), con riferimento alle concentrazioni di ammoniaca letale in base al PH e ai tempi di esposizione. Lo studio riporta delle rilevazioni a temperatura fissa di 30°C e che causino la morte di almeno il 50% degli animali in vasca. È riportata un’esposizione breve di un’ora e un’esposizione lunga di 4 giorni. Si chiamano valori LC50 (Lethal Concentration 50). Nelle nostre vasche bisognerà considerare dei margini di sicurezza ancora più ampi per avere la certezza di non combinare disastri e causare mortalità anche in considerazione della sensibilità delle nostre caridine e della loro scarsa tollerabilità.
Vi sono degli studi, però, che dimostrano come a PH acido sia necessario meno NH3 per produrre i suoi effetti tossici!
Questo vuol dire che dobbiamo monitorare anche e soprattutto le vasche con PH acidi (5,5-6,5) e temperature medie (18-23°C); vasche come quelle delle nostre caridine.
Nell’allevamento dei gamberi, per molte specie, è necessario dotarsi di un fondo allofano. La capacità tampone del fondo ci permetterà di avere un KH a 0, max 1 e il PH di solito si attesta su valori abbastanza bassi, quindi su valori di acidità, tra 5,5 e 6,5.
Si tratta di fattori molto importanti e che influiscono in modo determinante nella gestione.
Mantenere il PH e il KH bassi può essere però pericoloso e bisogna quindi adottare comportamenti idonei a evitare incidenti di percorso. Una semplice procedura come un repentino cambio con acqua a PH leggermente più elevato può provocare una conversione immediata dell'ammonio (NH4) in ammoniaca mortale (NH3) con risultati disastrosi.
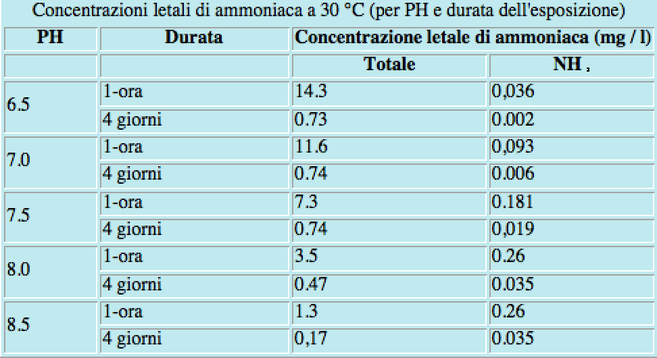
Di seguito una tabella che riporta i risultati di uno studio su una specie di salmone piuttosto delicato e sensibile (EPA, 1985), con riferimento alle concentrazioni di ammoniaca letale in base al PH e ai tempi di esposizione. Lo studio riporta delle rilevazioni a temperatura fissa di 30°C e che causino la morte di almeno il 50% degli animali in vasca. È riportata un’esposizione breve di un’ora e un’esposizione lunga di 4 giorni. Si chiamano valori LC50 (Lethal Concentration 50). Nelle nostre vasche bisognerà considerare dei margini di sicurezza ancora più ampi per avere la certezza di non combinare disastri e causare mortalità anche in considerazione della sensibilità delle nostre caridine e della loro scarsa tollerabilità.
Come avrete notato la quantità di NH3 è fortemente legata al PH.
Per chiarire meglio questo concetto analizziamo nel dettaglio la tabella:
Ma, abbiamo notato quanta ammoniaca NH3 è presente nel valore totale rilevato?
Che a PH alcalino basterà una concentrazione totale di ammoniaca bassa a causare la morte dei nostri animali, ma è altrettanto vero che a PH acido basterà pochissima NH3 per causare un disastro.
Riassumendo, se a PH 8,5 con una concentrazione di NH3 a 0,260 mg/L metà dei salmoni è morta, con lo stesso valore a PH 6,5 avremmo avuto la morte sicura di tutta la popolazione!
È altrettanto evidente che con l’aumentare del PH lo ione ammonio NH4 tende a mutare in NH3.
La relazione fra ammoniaca e ammonio è controllata dalla seguente equazione chimica:
Per chiarire meglio questo concetto analizziamo nel dettaglio la tabella:
- a PH 6,5 la concentrazione totale di ammoniaca è di 14,3 mg/L
- a PH 8,5 la concentrazione totale di ammoniaca è di 1,3 mg/L.
Ma, abbiamo notato quanta ammoniaca NH3 è presente nel valore totale rilevato?
- a PH 6,5 la concentrazione di NH3 è di 0,036 mg/L
- a PH 8,5 la concentrazione di NH3 è di 0,260 mg/L.
Che a PH alcalino basterà una concentrazione totale di ammoniaca bassa a causare la morte dei nostri animali, ma è altrettanto vero che a PH acido basterà pochissima NH3 per causare un disastro.
Riassumendo, se a PH 8,5 con una concentrazione di NH3 a 0,260 mg/L metà dei salmoni è morta, con lo stesso valore a PH 6,5 avremmo avuto la morte sicura di tutta la popolazione!
È altrettanto evidente che con l’aumentare del PH lo ione ammonio NH4 tende a mutare in NH3.
La relazione fra ammoniaca e ammonio è controllata dalla seguente equazione chimica:
Quando il pH è acido, la reazione è diretta verso destra, mentre quando è basico è diretta verso sinistra.
Le concentrazioni riportate sopra causano la morte al 50% del campione di animali a disposizione e all’altro 50% causa perdita di equilibrio, aumento della respirazione, diminuzione dell'escrezione di azoto, etc…
A concentrazioni più basse, l'ammoniaca ha comunque degli effetti dannosi, per esempio: una schiusa ridotta e tassi di crescita ridotti.
Come eliminare l’eventuale eccesso di ammoniaca?
Possiamo fare dei cambi d’acqua abbondanti facendo però attenzione al valore del PH e alla temperatura, perché, come abbiamo già detto, questi fattori influenzano la mutazione dello ione ammonio in ammoniaca.
L'agitazione superficiale può causare l'evaporazione di alcuni ioni dell’ammoniaca, ma non abbastanza rapidamente da essere efficace e riportare il valore in sicurezza.
La migliore soluzione è capire la ragione dell’ammoniaca rilevabile vasca e quindi risolvere il problema all’origine: filtro non maturo, filtro sporco, filtro sottodimensionato, collasso del filtro…etc…?
Le concentrazioni riportate sopra causano la morte al 50% del campione di animali a disposizione e all’altro 50% causa perdita di equilibrio, aumento della respirazione, diminuzione dell'escrezione di azoto, etc…
A concentrazioni più basse, l'ammoniaca ha comunque degli effetti dannosi, per esempio: una schiusa ridotta e tassi di crescita ridotti.
Come eliminare l’eventuale eccesso di ammoniaca?
Possiamo fare dei cambi d’acqua abbondanti facendo però attenzione al valore del PH e alla temperatura, perché, come abbiamo già detto, questi fattori influenzano la mutazione dello ione ammonio in ammoniaca.
L'agitazione superficiale può causare l'evaporazione di alcuni ioni dell’ammoniaca, ma non abbastanza rapidamente da essere efficace e riportare il valore in sicurezza.
La migliore soluzione è capire la ragione dell’ammoniaca rilevabile vasca e quindi risolvere il problema all’origine: filtro non maturo, filtro sporco, filtro sottodimensionato, collasso del filtro…etc…?
- Home
- I miei acquari
- Fai da te
-
Caridine
- Anatomia
- Alimentazione
- Dimorfismo sessuale e riproduzione
- Il caridinaio e i parametri ideali
- L'ambientamento delle caridine e gli accessori
- La classificazione e la selezione - DAVIDI...
- La classificazione e la selezione - LOGEMANNI
- La classificazione e la selezione - MARIAE
- La classificazione e la selezione - TAIWAN BEE
- Piante e Muschi
- CHIMICA
- ABOUT